염화 구리(I)
 | |
 | |
| 이름 | |
|---|---|
| IUPAC 이름 Copper(I) chloride | |
| 별칭 Cuprous chloride | |
| 식별자 | |
| |
3D 모델 (JSmol) |
|
바일슈타인 레퍼런스 | 8127933 |
| ChEBI |
|
| ChemSpider |
|
| DrugBank |
|
| ECHA InfoCard | 100.028.948 |
| EC 번호 |
|
| 13676 | |
PubChem CID |
|
| RTECS 번호 |
|
| UNII |
|
CompTox Dashboard (EPA) |
|
| |
SMILES
| |
| 성질 | |
| CuCl | |
| 몰 질량 | 98.999 g/mol[1] |
| 겉보기 | white powder, slightly green from oxidized impurities |
| 밀도 | 4.14 g/cm3[1] |
| 녹는점 | 423 °C (793 °F; 696 K)[1] |
| 끓는점 | 1,490 °C (2,710 °F; 1,760 K) (decomposes)[1] |
| 0.047 g/L (20 °C)[1] | |
용해도곱 (Ksp) | 1.72×10−7 |
| 용해도 | insoluble in ethanol, acetone;[1] soluble in concentrated HCl, NH4OH |
| 띠간격 | 3.25 eV (300 K, direct)[2] |
자화율 (χ) | -40.0·10−6 cm3/mol[3] |
굴절률 (nD) | 1.930[4] |
| 구조 | |
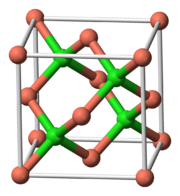
| Zincblende, cF20 | |
| F43m, No. 216[5] | |
격자 상수 | a = 0.54202 nm |
단위 세포 부피 (V) | 0.1592 nm3 |
단위 세포 화학식 (Z) | 4 |
| 위험 | |
| 물질 안전 보건 자료 | JT Baker |
| GHS 그림문자 |   |
| 신호어 | 경고 |
GHS 유해위험문구 | H302, H400, H410 |
GHS 예방조치문구 | P264, P270, P273, P301+312, P330, P391, P501 |
| NFPA 704 (파이어 다이아몬드) |  0 3 0 |
| 인화점 | Non-flammable |
| 반수 치사량 또는 반수 치사농도 (LD, LC): | |
LD50 (median dose) | 140 mg/kg |
| NIOSH (미국 건강 노출 한계): | |
PEL (허용) | TWA 1 mg/m3 (as Cu)[6] |
REL (권장) | TWA 1 mg/m3 (as Cu)[6] |
IDLH (직접적 위험) | TWA 100 mg/m3 (as Cu)[6] |
| 관련 화합물 | |
다른 음이온 | Copper(I) fluoride Copper(I) bromide Copper(I) iodide |
다른 양이온 | Silver(I) chloride Gold(I) chloride |
관련 화합물 | Copper(II) chloride |
달리 명시된 경우를 제외하면, 표준상태(25 °C [77 °F], 100 kPa)에서 물질의 정보가 제공됨.  예 확인 (관련 정보 예 확인 (관련 정보  예 예 아니오 ?) 아니오 ?) 정보상자 각주 | |
염화 구리(I)(Copper(I) chloride)는 화학식 CuCl을 갖는 구리의 염화 이온이다. 이 물질은 물에 겨우 녹는 백색 고체이지만 고농축 염산에는 매우 잘 녹는다. 염화 구리(II)(CuCl2)의 존재로 인해 불순물 견본이 녹색으로 나타난다.[7]
역사
로버트 보일이 17세기 중순에 처음 준비하였다.
- HgCl2 + 2 Cu → 2 CuCl + Hg
각주
- ↑ 가 나 다 라 마 바 Haynes, William M., 편집. (2011). 《CRC Handbook of Chemistry and Physics》 92판. Boca Raton, FL: CRC Press. 4.61쪽. ISBN 1439855110.
- ↑ Garro, Núria; Cantarero, Andrés; Cardona, Manuel; Ruf, Tobias; Göbel, Andreas; Lin, Chengtian; Reimann, Klaus; Rübenacke, Stefan; Steube, Markus (1996). “Electron-phonon interaction at the direct gap of the copper halides”. 《Solid State Communications》 98 (1): 27–30. Bibcode:1996SSCom..98...27G. doi:10.1016/0038-1098(96)00020-8.
- ↑ Haynes, William M., 편집. (2011). 《CRC Handbook of Chemistry and Physics》 92판. Boca Raton, FL: CRC Press. 4.132쪽. ISBN 1439855110.
- ↑ Patnaik, Pradyot (2002) Handbook of Inorganic Chemicals. McGraw-Hill, ISBN 0-07-049439-8
- ↑ Hull, S.; Keen, D. A. (1994). “High-pressure polymorphism of the copper(I) halides: A neutron-diffraction study to ~10 GPa”. 《Physical Review B》 50 (9): 5868–5885. Bibcode:1994PhRvB..50.5868H. doi:10.1103/PhysRevB.50.5868. PMID 9976955.
- ↑ 가 나 다 NIOSH Pocket Guide to Chemical Hazards. “#0150”. 미국 국립 직업안전위생연구소 (NIOSH).
- ↑ Pastor, Antonio C. (1986) 미국 특허 4,582,579 "Method of preparing cupric ion free cuprous chloride" Section 2, lines 4–41.
외부 링크
- National Pollutant Inventory – Copper and compounds fact sheet
- The COPureSM Process for purifying CO utilizing a copper chloride complex
- v
- t
- e
염화물(Cl-)
| HCl(aq) | He | ||||||||||||||||||||
| LiCl | BeCl2 | BCl3 B2Cl4 +BO3 | C2Cl2 C2Cl4 C2Cl6 CCl4 | NCl3 ClN3 | ClxOy Cl2O Cl2O2 ClO ClO2 Cl2O4 Cl2O6 Cl2O7 ClO4 | ClF ClF3 ClF5 | Ne | ||||||||||||||
| NaCl | MgCl2 | AlCl AlCl3 | Si2Cl6 SiCl4 | P2Cl4 PCl3 PCl5 | S2Cl2 SCl2 SCl4 | Cl2 | Ar | ||||||||||||||
| KCl | CaCl CaCl2 | ScCl3 | TiCl2 TiCl3 TiCl4 | VCl2 VCl3 VCl4 VCl5 | CrCl2 CrCl3 CrCl4 | MnCl2 MnCl3 | FeCl2 FeCl3 | CoCl2 CoCl3 | NiCl2 | CuCl CuCl2 | ZnCl2 | GaCl GaCl3 | GeCl2 GeCl4 | AsCl3 AsCl5 | Se2Cl2 SeCl2 SeCl4 | BrCl | Kr | ||||
| RbCl | SrCl2 | YCl3 | ZrCl3 ZrCl4 | NbCl3 NbCl4 NbCl5 | MoCl2 MoCl3 MoCl4 MoCl5 MoCl6 | TcCl3 TcCl4 | RuCl2 RuCl3 RuCl4 | RhCl3 | PdCl2 | AgCl | CdCl2 | InCl InCl2 InCl3 | SnCl2 SnCl4 | SbCl3 SbCl5 | Te3Cl2 TeCl2 TeCl4 | ICl ICl3 | XeCl XeCl2 XeCl4 | ||||
| CsCl | BaCl2 | * | LuCl3 | HfCl4 | TaCl5 | WCl2 WCl3 WCl4 WCl5 WCl6 | ReCl3 ReCl4 ReCl5 ReCl6 | OsCl2 OsCl3 OsCl4 OsCl5 | IrCl2 IrCl3 IrCl4 | PtCl2 PtCl4 | AuCl (Au[AuCl4])2 AuCl3 | Hg2Cl2 HgCl2 | TlCl TlCl3 | PbCl2 PbCl4 | BiCl3 | PoCl2 PoCl4 | AtCl | Rn | |||
| FrCl | RaCl2 | ** | LrCl3 | RfCl4 | DbCl5 | SgO2Cl2 | BhO3Cl | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||
| * | LaCl3 | CeCl3 | PrCl3 | NdCl2 NdCl3 | PmCl3 | SmCl2 SmCl3 | EuCl2 EuCl3 | GdCl3 | TbCl3 | DyCl2 DyCl3 | HoCl3 | ErCl3 | TmCl2 TmCl3 | YbCl2 YbCl3 | |||||||
| ** | AcCl3 | ThCl4 | PaCl4 PaCl5 | UCl3 UCl4 UCl5 UCl6 | NpCl3 | PuCl3 | AmCl2 AmCl3 | CmCl3 | BkCl3 | CfCl3 | EsCl2 EsCl3 | FmCl2 | MdCl2 | NoCl2 | |||||||



