Acid sulfamic
| Acid sulfamic | |
 | |
 | |
| Identificare | |
|---|---|
SMILES NS(=O)(=O)O[1]  | |
| Număr CAS | 5329-14-6 |
| ChEMBL | CHEMBL68253 |
| PubChem CID | 19366655, 134939864 5987, 19366655, 134939864 |
| Formulă chimică | H₃NO₃S[1]  |
| Masă molară | 97 u.a.m.[1]  |
| Sunt folosite unitățile SI și condițiile de temperatură și presiune normale dacă nu s-a specificat altfel. | |
Modifică date / text  | |
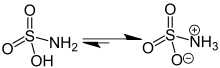
Acidul sulfamic (denumit și acid amidosulfonic, acid amidosulfuric, acid aminosulfonic și acid sulfamidic) este un compus chimic cu formula chimică H3NSO3. Este un compus incolor, hidrosolubil, cu diverse aplicații industriale. Se topește la 205 °C iar la temperaturi mai mari se descompune în apă, trioxid de sulf și azot molecular.[2] Sărurile sale se numesc sulfamați.
Obținere
Acidul sulfamic este obținut la nivel industrial în urma reacției dintre uree și un amestec de trioxid de sulf și acid sulfuric (cunoscut sub denumirea de oleum). Procesul are loc în două etape, prima fiind cea de sulfamare:
Prin această metodă, aproximativ 96.000 de tone de acid sulfamic au fost produse în anul 1995.[3]
Note
- ^ a b c „Acid sulfamic”, SULFAMIC ACID (în engleză), PubChem, accesat în
- ^ Yoshikubo, K.; Suzuki, M. (). „Sulfamic Acid and Sulfamates”. Kirk-Othmer Encyclopedia of Chemical Technology. doi:10.1002/0471238961.1921120625151908.a01. ISBN 0471238961.
- ^ Metzger, A. (), „Sulfamic Acid”, Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, doi:10.1002/14356007.a25_439












