Supersyra
 | Den här artikeln behöver källhänvisningar för att kunna verifieras. (2010-09) Åtgärda genom att lägga till pålitliga källor (gärna som fotnoter). Uppgifter utan källhänvisning kan ifrågasättas och tas bort utan att det behöver diskuteras på diskussionssidan. |
Supersyror kallas de syror som är starkare än 100 % svavelsyra. Enligt modern definition är en supersyra ett medium där den kemiska potentialen för protonen är högre än i ren svavelsyra.
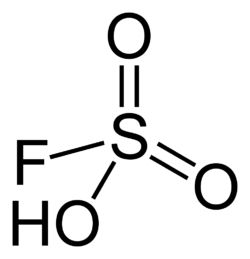
Supersyror är betydelsefulla inom organisk kemi. Två supersyror som är kommersiellt tillgängliga är trifluorometansulfonsyra (CF3SO3H) och fluorsvavelsyra (HSO3F). Båda dessa supersyror är tusen gånger starkare än svavelsyra. Lewissyra och Brønstedsyra är två syror som ofta kombineras för att förbereda starkare supersyror, bland annat fluoroantimonisk syra som är ca en miljon miljarder gånger starkare/surare än 100 % ren svavelsyra.
Karboransyror är en annan grupp supersyror, vilka också hör till de starkaste supersyror man känner till. Karboransyra går att lagra på glasflaska, vilket är ovanligt då de flesta supersyror fräter igenom glaskärl. Man tror att karboransyran kan få en tillämpning vid utveckling av vitaminpreparat och syrade organiska molekyler.
Historia
1927 bestämde James Bryant Conant att termen supersyra skulle innefatta alla syror som var starkare än konventionella mineralsyror. Definitionen ändrades senare av Ronald Gillespie år 1971 till dagens definition. År 1994 fick den ungersk-amerikanske kemisten George A. Olah nobelpriset "för sina bidrag till karbokatjonernas kemi", och därmed också till framställningen av supersyror.
Referenser
- Den här artikeln är helt eller delvis baserad på material från engelskspråkiga Wikipedia, Superacid, 16 februari 2019.










